Using clusters of tiny magnetic particles about 1,000 times smaller than the width of a human hair, researchers from the UCLA Henry Samueli School of Engineering and Applied Science have shown that they can manipulate how thousands of cells divide, morph and develop finger-like extensions.
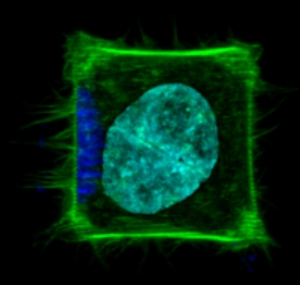 A cell patterned to adhere to the shape of a square with localized nanoparticles (dark blue) causing local generation of actin-rich filopodia (green). Nucleus (cyan) is also shown. The cell size is ~ 30 micrometers.
A cell patterned to adhere to the shape of a square with localized nanoparticles (dark blue) causing local generation of actin-rich filopodia (green). Nucleus (cyan) is also shown. The cell size is ~ 30 micrometers.
This new tool could be used in developmental biology to understand how tissues develop, or in cancer research to uncover how cancer cells move and invade surrounding tissues, the researchers said.
The UCLA team's findings were published online Oct. 14 in the journal Nature Methods.
A cell can be considered a complex biological machine that receives an assortment of "inputs" and produces specific "outputs," such as growth, movement, division or the production of molecules. Beyond the type of input, cells are extremely sensitive to the location of an input, partly because cells perform "spatial multiplexing," reusing the same basic biochemical signals for different functions at different locations within the cell.
Understanding this localization of signals is particularly challenging because scientists lack tools with sufficient resolution and control to function inside the miniature environment of a cell. And any usable tool would have to be able to perturb many cells with similar characteristics simultaneously to achieve an accurate distribution of responses, since the responses of individual cells can vary.
To address this problem, an interdisciplinary UCLA team that included associate professor of bioengineering Dino Di Carlo, postdoctoral scholar Peter Tseng and professor of electrical engineering Jack Judy developed a platform to precisely manipulate magnetic nanoparticles inside uniformly shaped cells. These nanoparticles produced a local mechanical signal and yielded distinct responses from the cells.
By determining the responses of thousands of single cells with the same shape to local nanoparticle-induced stimuli, the researchers were able to perform an automated averaging of the cells' response.
To achieve this platform, the team first had to overcome the challenge of moving such small particles (each measuring 100 nanometers) through the viscous interior of a cell once the cells engulfed them. Using ferromagnetic technologies, which enable magnetic materials to switch "on" and "off," the team developed an approach to embed a grid of small ferromagnetic blocks within a microfabricated glass slide and to precisely place individual cells in proximity to these blocks with a pattern of proteins that adhere to cells.
When an external magnetic field is applied to this system, the ferromagnetic blocks are switched "on" and can therefore pull the nanoparticles within the cells in specific directions and uniformly align them. The researchers could then shape and control the forces in thousands of cells at the same time.
Using this platform, the team showed that the cells responded to this local force in several ways, including in the way they divided. When cells go through the process of replication to create two cells, the axis of division depends on the shape of the cell and the anchoring points by which the cell holds on to the surface. The researchers found that the force induced by the nanoparticles could change the axis of cell division such that the cells instead divided along the direction of force.
The researchers said this sensitivity to force may shed light on the intricate forming and stretching of tissues during embryonic development. Besides directing the axis of division, they found that nanoparticle-induced local force also led to the activation of a biological program in which cells generate filopodia, which are finger-like, actin-rich extensions that cells often use to find sites to adhere to and which aid in movement.
Di Carlo, the principal investigator on the research, envisions that the technique can apply beyond the control of mechanical stimuli in cells.
"Nanoparticles can be coated with a variety of molecules that are important in cell signaling," he said. "We should now have a tool to quantitatively investigate how the precise location of molecules in a cell produces a specific behavior. This is a key missing piece in our tool-set for understanding cell programs and for engineering cells to perform useful functions."
Di Carlo and the team are also associated with UCLA's California NanoSystems Institute and Jonsson Comprehensive Cancer Center. The work was funded by the National Institutes of Health through an NIH Director's New Innovator Award.
Source: http://www.ucla.edu