Nov 14 2012
Tumor cells circulating in a patient’s bloodstream can yield a great deal of information on how a tumor is responding to treatment and what drugs might be more effective against it. But first, these rare cells have to be captured and isolated from the many other cells found in a blood sample.
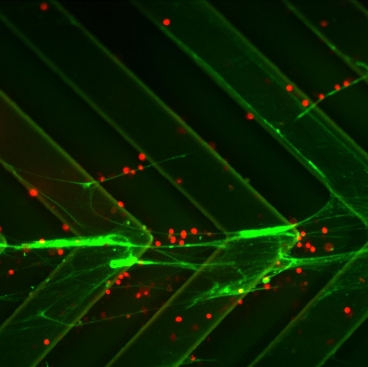 Cells traveling through a microfluidic device can be trapped by strands of DNA (green). Image: Suman Bose and Chong Shen
Cells traveling through a microfluidic device can be trapped by strands of DNA (green). Image: Suman Bose and Chong Shen
Many scientists are now working on microfluidic devices that can isolate circulating tumor cells (CTCs), but most of these have two major limitations: It takes too long to process a sufficient amount of blood, and there is no good way to extract cancer cells for analysis after their capture.
A new device from researchers at MIT and Brigham and Women’s Hospital overcomes those obstacles. Inspired by the tentacles of a jellyfish, the team coated a microfluidic channel with long strands of DNA that grab specific proteins found on the surfaces of leukemia cells as they flow by. Using this strategy, the researchers achieved flow rates 10 times higher than existing devices — fast enough to make the systems practical for clinical use.
Using this technology, described in this week’s issue of the Proceedings of the National Academy of Sciences, doctors could monitor cancer patients to determine whether their treatment is working.
“If you had a rapid test that could tell you whether there are more or less of these cells over time, that would help to monitor the progression of therapy and progression of the disease,” says Jeff Karp, an associate professor of medicine at Harvard Medical School and co-director of the Center for Regenerative Therapeutics at Brigham and Women’s Hospital in Boston.
This type of device could also enable personalized treatments: Once cells are isolated from a patient, doctors could test different drugs on them to determine which are most effective.
On the hunt for rare cancer cells
The new technology grew out of a collaboration between Karp’s lab and that of Rohit Karnik, an associate professor of mechanical engineering at MIT. Lead authors of the paper are Weian Zhao, a former postdoc in Karp’s lab and now an assistant professor at the University of California at Irvine; Cheryl Cui, a graduate student in the Harvard-MIT Division of Health Sciences and Technology; and Suman Bose, a graduate student in Karnik’s lab.
DNA ‘tentacles’
The number of CTCs found in a milliliter of a particular patient’s blood can range from just a few to several thousand. To isolate those rare cells, researchers have tried building microfluidic channels dotted with antibodies specific to a protein found on the target cells. However, because the antibodies only extend tens of nanometers from the bottom of the channel, the capture of cells by the antibodies is slow.
To extend the reach of the capture molecules, Karp and Karnik’s team mimicked the tentacles of jellyfish, creating long strands of repeating DNA sequences. Those sequences, known as aptamers, target a protein found in large numbers on leukemia cells.
The DNA strands are attached to a microchannel with a herringbone pattern on its floor. Those patterned ridges cause the blood to swirl as it flows through the channel, improving the chances that individual cells will come into contact with the tentacles, which extend hundreds of microns into the channel. This allows the researchers to increase the rate of blood flow.
“Normally what happens at high flow rates is the cells don’t really come close to the surface, and it’s very challenging to capture the target cells,” Karnik says. “But this combination of these herringbone grooves to mix the solution and bring the cells into contact with surfaces, plus having aptamers that are sticking out into the solution, enables very high capture rates at very high flow rates.”
Flow rates in the new device are 10 times higher than those reported for previous devices, and the system can capture 60 to 80 percent of the target cells. In the current model, which measures 1 square centimeter, the flow rate is 1 milliliter per hour. By making the device larger, the researchers say they could boost the flow rate to 100 milliliters of blood per hour — fast enough to rapidly process the 10- to 20-milliliter samples that would be needed to get an accurate CTC count from an individual patient.
Because the “tentacles” are made of DNA, they can easily be cleaved with enzymes, freeing the captured cells for further analysis.
Peter Kuhn, an associate professor of cell biology at the Scripps Research Institute, says this technology is an interesting alternative to existing approaches to capture rare cells, adding that further testing is needed to validate the technology’s usefulness.
“This field needs many different avenues for rare-cell identification to be explored,” Kuhn says. “These technologies can provide the key enablers for studying disease in humans.”
Minimally invasive
Devices that capture CTCs could offer a better alternative to sampling bone marrow in determining whether cancer treatment is working in a leukemia patient.
“If one could improve the sensitivity of detection in blood, then this approach may enable a transition from isolating marrow to isolating blood, which is much less invasive and you can do it more often. It could change the paradigm for how residual disease is detected,” Karp says.
“The beauty of this technology is its versatility,” Zhao says. “You can easily modify the length and density of the DNA chains; you can include different sequences in the DNA to capture different types of cells.”
This feature makes it a platform technology that can be broadly applied in the clinic and research laboratories. For instance, another possible application is capturing fetal cells, which are very rare in a pregnant woman’s bloodstream. Analyzing these cells could help doctors perform prenatal diagnostic tests for a range of diseases using an approach that is far less invasive than amniocentesis.
The researchers are now working on adapting the DNA strands to target other molecules, such as receptors found on the surfaces of cells dislodged from solid tumors.
Source: http://www.mit.edu/